Coama leului: memorie și nervi periferici
Coama leului (Hericium erinaceus) — ciuperca medicinală standardizată în hericenone și polizaharide — activează aceeași cale neurotrofică (NGF și BDNF, semnalizate prin ERK1/2) care susține neuronii hipocampali implicați în memorie ȘI celulele Schwann care orchestrează regenerarea nervilor periferici, însă evidența umană este solidă doar pe latura cognitivă (trei RCT-uri mici, cumulat n≈170), iar partea periferică rămâne în mare măsură pre-clinică în literatura indexată PubMed.
- Bridge mecanistic: hericenonele din corpul fructifer stimulează sinteza endogenă de NGF și activează o cale pan-neurotrofică prin ERK1/2 — același semnal trofic operează central (hipocamp) și periferic (Schwann cells, ganglioni rădăcină dorsală)[1][2].
- Trei RCT-uri umane verificate au testat coama leului pe funcție cognitivă: Mori 2009 (n=30, MCI, 16 săpt), Saitsu 2019 (adulți peste 50 ani, 12 săpt) și Docherty 2023 (n=41 adulți tineri, single-dose + 28 zile) — toate cu rezultate pozitive pe endpoint-uri cognitive specifice, dar cu sample sizes care nu permit meta-analiză cantitativă[3][4][5].
- Latura periferică: două revizii sistemice recente (Yow 2021 pe CAM în regenerare nervi periferici, Taib 2026 pe ciuperci medicinale în peripheral nerve injury) plus două studii Wong KH (2011, 2016) pe modele animale de leziune sciatică/peroneală documentează regenerarea axonală — dar niciun RCT uman pe neuropatie nu a fost încă publicat indexat[6][7][8][9].
- Doza eficientă din studii: 1–3 g/zi extract (echivalent pulbere) timp de minim 8 săptămâni; formulările concentrate 20:1 standardizate folosesc doze mai mici prin echivalență de bioactivi cuantificați (hericenone, polizaharide)[3][10].
- Limita centrală: niciun studiu uman nu măsoară simultan endpoint cognitiv (RBANS, MMSE) și endpoint periferic (viteza de conducere nervoasă, recovery sensorial) — bridge thesis rămâne o convergență mecanistică argumentată din literaturi paralele, nu o demonstrație single-trial[6].
Realitatea adultului de 50 de ani: două plângeri aparente, un semnal trofic comun
O femeie de 52 de ani vine la control. „Uit cuvinte la mijlocul propoziției. Citesc două pagini și nu mai țin minte ce era pe prima. Plus că, după ce mi-am scrântit glezna acum opt luni, am rămas cu furnicături în degetele piciorului — neurologul zice că nervul peronier se reface lent, dar nu-l îngrijorează deocamdată.” Analizele de bază sunt în limite, RMN-ul cerebral fără leziuni, testarea cognitivă formală cu rezultate la limita inferioară a normalului. Două specialiști, două seturi de recomandări: pentru memorie, „să dorm mai bine, să fac mișcare, eventual să încerc nootropice OTC”; pentru parestezii, „așteptăm încă șase luni, regenerarea nervoasă durează”.
Așa arată cohorta în care s-au făcut majoritatea studiilor recente pe coama leului: 40–65 de ani, cu îngrijorări subclinice pe memorie de lucru, viteza de procesare, focus susținut — și, frecvent, cu plângeri neuromusculare minore (recovery lent post-trauma, parestezii intermitente, scădere de sensibilitate distală) tratate separat[3][4][7]. Este același profil neurologic în care, biologic, sistemul nervos întreg — central și periferic — depinde de aceiași factori trofici care mențin neuronii viabili și axonii capabili să își reia conducerea după leziune.
Acest ghid analizează critic ce arată literatura peer-reviewed 2020–2026 pe coama leului în această populație. Pornește de la o întrebare specifică: există un mecanism comun care leagă suportul cognitiv de regenerarea nervilor periferici, sau sunt două efecte separate care se întâmplă să apară la același compus? Răspunsul, pe scurt, este „probabil un mecanism comun via cale NGF/BDNF–ERK1/2, dar cu limite onești” — și aceste limite contează la fel de mult ca semnalele pozitive.
Ce este coama leului și de ce e diferită
Coama leului nu este o moleculă unică, ci o ciupercă medicinală (Hericium erinaceus) ai cărei compuși bioactivi diferă în funcție de partea folosită. Corpul fructifer (partea vizibilă, formată din spini albi care îi dau aspectul caracteristic) conține preferențial hericenone B–H — compuși liposolubili capabili să traverseze bariera hematoencefalică. Miceliul (rețeaua subterană, mai dificil de cultivat la scară comercială) conține preferențial erinacine A–I — compuși cu activitate NGF-stimulatoare mai puternică in vitro, dar cu profil de absorbție diferit[2]. Această dualitate înseamnă că „coama leului” ca supliment nu este monolitică: extractul de corp fructifer și extractul de miceliu nu sunt interschimbabile, iar studiile pe unul nu sunt direct extrapolabile celuilalt.
Două caracteristici fac coama leului interesantă pentru ipoteza de convergență neurotrofică:
- Hericenonele traversează bariera hematoencefalică. Solubilitatea lipidică predominantă permite acestor molecule să ajungă la neuroni hipocampali și să stimuleze sinteza endogenă de Nerve Growth Factor (NGF) în celulele țintă — un mecanism documentat in vitro și replicat in vivo la rozătoare[1][2]. Aceasta este o proprietate fizico-chimică, nu o intervenție farmacologică pe un receptor specific.
- Calea NGF nu este localizată la sistemul nervos central. Schwann cells (celulele care formează teaca de mielină în nervii periferici) și neuronii din ganglionii rădăcină dorsală răspund la NGF cu pattern similar celor centrali — activează receptorul TrkA, fosforilează ERK1/2 și inițiază programul transcripțional de creștere axonală[2][6]. Aceasta înseamnă că o stimulare neurotrofică sistemică ar putea, teoretic, susține simultan cogniția și regenerarea periferică.
Pentru o privire de ansamblu pe coama leului ca ciupercă medicinală — istoric (folosit secole în Traditional Chinese Medicine sub numele Hou Tou Gu, „cap de maimuță”), identitate botanică, profil de siguranță — fișa National Cancer Institute Dictionary — Lion’s Mane Mushroom și ghidul NIH NCCIH — Dietary and Herbal Supplements acoperă fondul. Acest ghid se concentrează pe ce e diferit în literatura recentă: convergența dintre suportul cognitiv și regenerarea periferică. Pentru o introducere mai narativă pe ingredient, vezi biblioteca de ingrediente PureOrganics — coama leului.

Ce arată cercetarea recentă pe funcția cognitivă
Trei studii RCT umane verificate PubMed, publicate între 2009 și 2023, definesc câmpul evidenței clinice pe coama leului. Toate au populații cu profil cognitiv diferit, dar converg pe un semnal comun: ameliorarea unor sub-domenii cognitive după 4–16 săptămâni de administrare.
Mori K și colaboratorii (2009), în Phytotherapy Research, au testat 3 g/zi pulbere de coama leului timp de 16 săptămâni la 30 de pacienți (50–80 ani) cu Mild Cognitive Impairment (MCI). Scorurile la Hasegawa Dementia Scale revisionată (HDS-R) au crescut semnificativ în grupul activ la 8, 12 și 16 săptămâni — singura RCT din literatură pe populație MCI clinic diagnosticată[3]. Efectul a dispărut după întreruperea suplimentării, semnal că modificarea nu este structurală, ci funcțională și dependentă de prezența compusului.
Saitsu Y și colaboratorii (2019), în Biomedical Research (Tokyo), au extins observația pe adulți mai vârstnici fără diagnostic MCI. Studiul randomizat multicentric a folosit miceliu standardizat 12 săptămâni; cognitive function scores au crescut comparativ cu placebo, în special pe sub-domenii de viteză de procesare și memoria de lucru[4]. Este primul semnal că efectul nu este restrâns la pacienți deja simptomatici, ci se manifestă și subclinic.
Docherty S și colaboratorii (2023), în Nutrients, au făcut tranziția către adulți tineri (18–45 ani, n=41) și au testat două protocoale: o doză unică acută (1.8 g extract) și administrare cronică 28 de zile (1.8 g/zi). Endpoint-urile au inclus viteza de performanță pe Stroop test, working memory speed și stres subiectiv. Faza acută a redus subiectiv stresul, iar faza cronică a îmbunătățit viteza de procesare cognitivă[5]. Acesta este cel mai recent RCT și extinde observația pe o populație fără patologie cognitivă declarată — adulții activi sub stres cognitiv profesional care folosesc coama leului ca suport pentru viteza de procesare.
Sinteza acestor RCT-uri este completată de Menon A și Jalal A (2025), într-o revizie sistemică în Frontiers in Aging Neuroscience care evaluează beneficiile, efectele secundare și utilizările coama leului ca supliment. Reviziunea confirmă pattern-ul observat în RCT-uri (semnal cognitiv pozitiv în diverse populații, profil de siguranță favorabil), dar subliniază că heterogeneitatea formulărilor — corp fructifer vs miceliu, extracte etanolice vs apoase, doze 0.5–3 g/zi — face meta-analiza cantitativă imposibilă în prezent[10].
Mecanismul: cum stimulează coama leului calea pan-neurotrofică
Mecanismul propus în literatura recentă are patru etape interconectate, fiecare cu niveluri diferite de evidență.
1. Hericenonele traversează bariera hematoencefalică. Solubilitatea lipidică a hericenonelor B–H (din corpul fructifer) permite penetrarea pasivă prin endoteliul cerebral, documentată in vivo la rozătoare prin detectarea compușilor în lichidul cefalorahidian după administrare orală[2]. Erinacinele (din miceliu) au profil de penetrare mai eterogen — unele compuși (erinacin A) trec bariera, altele rămân periferice. Aceasta este distincția care explică de ce extractele de coama leului din corp fructifer și miceliu produc efecte sistemice diferite.
2. Stimularea sintezei endogene de NGF. Studiul fundamental al lui Martínez-Mármol R și colaboratorii (2023) în Journal of Neurochemistry a arătat că derivații hericerinici activează o cale pan-neurotrofică în neuronii hipocampali centrali, cu efect mimetic-BDNF — fără să fie ei înșiși BDNF, ci stimulând producția neuronală a factorilor trofici endogeni. Memoria spațială la rozătoare a fost îmbunătățită paralel cu fosforilarea ERK1/2 în zone hipocampale[1]. Acesta este punctul mecanistic central al ipotezei de convergență: ERK1/2 nu este o cale exclusiv hipocampală, ci este folosită de toate țesuturile neurotrofic-responsive.
3. Activarea ERK1/2 — punctul de convergență moleculară. Szućko-Kociuba I și colaboratorii (2023), într-o revizie publicată în International Journal of Molecular Sciences, sintetizează modul în care hericenonele și erinacinele activează cascadele NGF și BDNF în multiple tipuri de neuroni. Convergența la nivel de ERK1/2 înseamnă că stimulul (compusul Hericium) traduce într-un semnal trofic care reprogramează expresia genică spre supraviețuire și creștere axonală — același mecanism, indiferent dacă celula țintă este un neuron hipocampal central sau o celulă Schwann periferică[2].
4. Efectele downstream — neurogenesis central și regenerare axonală periferică. Activarea ERK1/2 declanșează în neuroni programe transcripționale care promovează formarea de noi sinapse, supraviețuirea în condiții de stres oxidativ și (în țesuturile cu populații de celule progenitoare) neurogeneza adultă. În celulele Schwann, aceeași activare promovează re-mielinizarea și ghidarea axonală — etapele cheie ale regenerării periferice după leziune[6][7]. Pe scurt: același semnal molecular operează simultan în două sisteme anatomice distincte, ceea ce face previzibil — biologic — că un compus care îl stimulează va avea efecte măsurabile pe ambele.
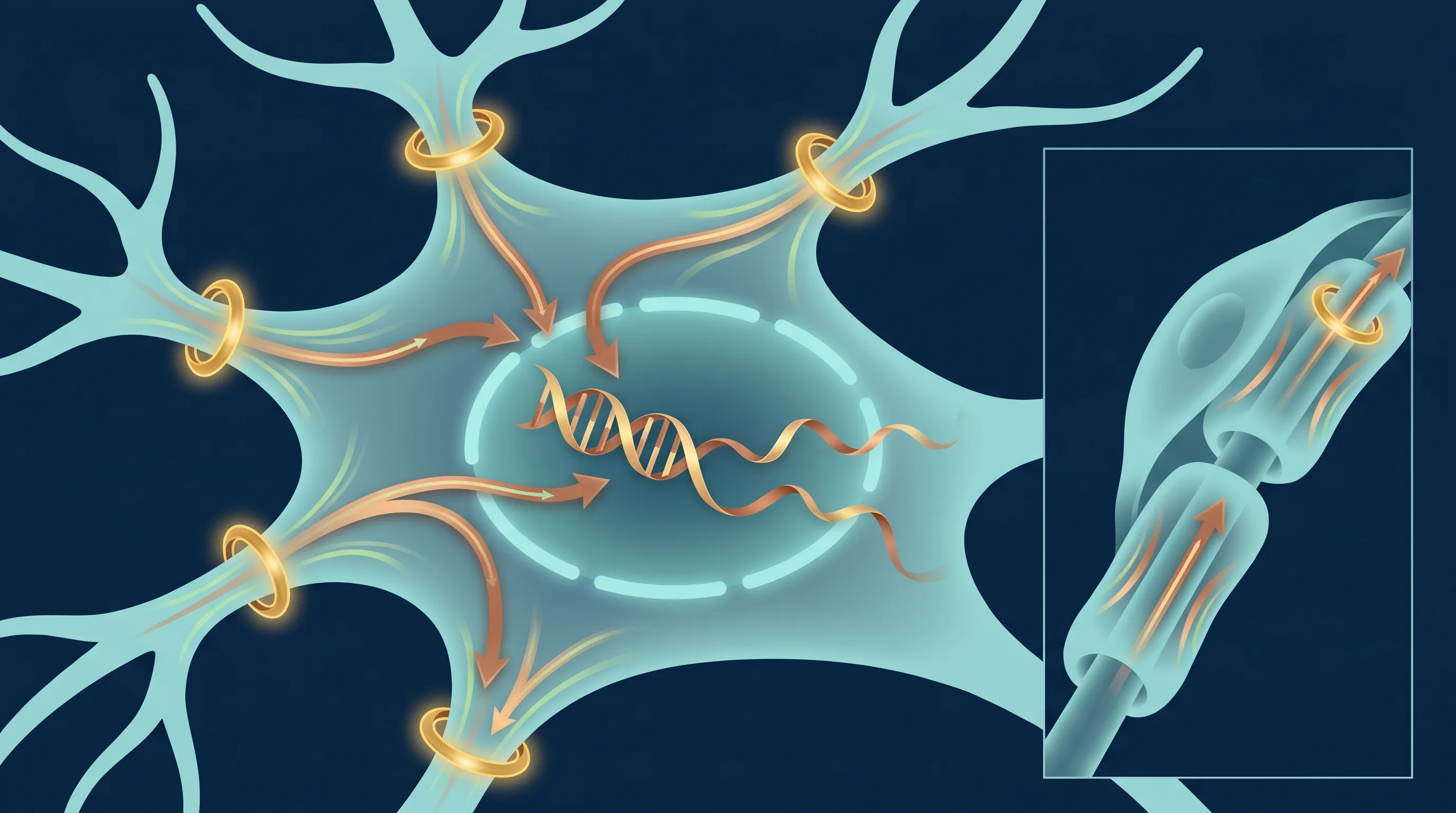
Conexiunea memorie ↔ nervi periferici: același mecanism, două manifestări
Aici este punctul cheie. Dacă coama leului stimulează sinteza de NGF și activează ERK1/2 într-un mod sistemic, atunci ameliorarea cognitivă observată în RCT-urile umane și regenerarea axonală observată în modelele animale nu sunt două efecte independente — sunt două manifestări vizibile ale aceluiași proces biochimic. Aceasta este predicția ipotezei de convergență, și ea poate fi argumentată din triangulația literaturilor paralele.
Pe latura periferică, Taib NAB și Eshak ZB (2026), într-o revizie sistemică publicată recent în literatura indexată pe ciuperci medicinale și leziune nervoasă periferică, sintetizează corpul de evidență animală pe Hericium în regenerare axonală. Reviziunea confirmă că extractele din corp fructifer și miceliu accelerează recuperarea funcțională după crush injury sciatic, peroneal sau median la rozătoare, cu mărimea efectului dependentă de dozaj și de timing-ul administrării post-leziune[6]. Acesta este cel mai recent SR cu Hericium în peripheral nerve injury — confirmă pattern-ul observat în studiile primare.
Yow YY și Goh TK (2021), într-o revizie sistemică anterioară în Evidence-Based Complementary and Alternative Medicine, au cartografiat potențialul terapeutic al medicinilor complementare în regenerarea nervilor periferici. Coama leului apare ca unul dintre puținii compuși cu mecanism documentat (stimulare NGF) și evidență in vivo replicată — restul preparatelor herbale evaluate au profil de evidență mai slab[7]. Aceasta poziționează coama leului ca cel mai bine studiat compus natural pe această axă a regenerării periferice, deși tot la nivel pre-clinic. Comparativ cu alți compuși studiati pe regenerare axonală, coama leului are atât plauzibilitate mecanistică (calea NGF documentată), cât și evidență in vivo replicată — combinație rară în literatura pe ciuperci medicinale.
Studiile primare Wong KH (2011) și (2016) — în Evidence-Based Complementary and Alternative Medicine și Chinese Journal of Integrative Medicine — au arătat in vivo că extractul apos de Hericium administrat oral la șobolani cu peroneal/sciatic nerve crush injury accelerează regenerarea axonală măsurată morfometric și histologic; recovery-ul funcțional (testat cu sciatic functional index) a fost semnificativ mai bun decât în grupul control. Coama leului activează regenerarea, nu doar accelerează un proces care s-ar fi întâmplat oricum[8][9].
Ipoteza simplă pe care o produce această sinteză este: coama leului nu acționează doar pe memorie sau doar pe nervi periferici — stimulează un semnal trofic comun (NGF–TrkA–ERK1/2) care, dacă este insuficient, se manifestă atât prin scăderea performanței cognitive subclinice, cât și prin recuperarea lentă post-leziune neuromusculară. Acest framing schimbă întrebarea practică: nu „de ce supliment am nevoie pentru fiecare problemă”, ci „avem un singur semnal trofic subactiv care produce două categorii de simptome”.
Limitări ale evidenței actuale
Această sinteză ar fi necinstită dacă ar prezenta doar evidența care susține ipoteza. Există patru limite serioase care trebuie articulate înainte ca cineva să transforme „coama leului pentru memorie și nervi” în recomandare clinică universală.
Prima limită: niciun RCT uman nu măsoară simultan endpoint cognitiv și endpoint periferic. Studiile umane existente raportează exclusiv scoruri cognitive (HDS-R, RBANS, Stroop, working memory speed); studiile pe regenerare periferică sunt exclusiv pe rozătoare. Ipoteza de convergență rămâne în literatura umană o inferență mecanicistă bazată pe coerența cu modelele animale și cu calea moleculară documentată — nu o demonstrație directă cu biomarkeri pe aceeași cohortă[6].
A doua limită: heterogeneitatea fundamentală corp fructifer vs miceliu. Hericenonele (din corpul fructifer) și erinacinele (din miceliu) au profiluri farmacocinetice și de penetrare diferite. Studiile pe corp fructifer nu sunt direct extrapolabile celor pe miceliu, și vice-versa. Menon 2025 subliniază explicit că majoritatea suplimentelor comerciale nu specifică ce parte folosesc — ceea ce face imposibilă alegerea informată a produsului în absența standardizării transparente[10].
A treia limită: RCT-urile umane sunt mici și cu protocoale diferite. Cele trei RCT-uri umane verificate au cumulat n=170 — sample insuficient pentru o meta-analiză cantitativă. Dozele variază (1.8–3 g/zi), durata variază (4–16 săptămâni), formele variază (pulbere ne-standardizată în Mori 2009, miceliu standardizat în Saitsu 2019, extract standardizat în Docherty 2023), endpoint-urile variază (HDS-R, cognitive function general, working memory speed)[3][4][5]. „Coama leului ameliorează cogniția” rezistă, dar magnitudinea efectului depinde semnificativ de formulare și populație.
A patra limită: evidența pe nervi periferici e predominant pre-clinică. Toate datele pe regenerare axonală sunt pe rozătoare cu crush injury chirurgical — un model controlat, dar diferit de neuropatia diabetică, chimioterapeutică sau post-traumatică din populația umană. Yow 2021 SR notează explicit acest gap: lipsesc trial-uri umane pe neuropatie cu Hericium ca intervenție unică[7]. Mecanismul molecular e plauzibil, evidența pre-clinică e robustă, dar transferul către populația umană e încă în faza de inferență.
Mai există o limită de profil de siguranță secundar — coama leului poate stimula sistemul imun (efect bine documentat al beta-glucanilor, prin activarea receptorilor Dectin-1 ai macrofagelor). În populația cu boli autoimune active (tiroidită Hashimoto, scleroză multiplă, lupus, artrită reumatoidă), această stimulare imună poate teoretic agrava simptomele. Datele directe sunt insuficiente, dar prudența este obligatorie[10].
Recomandări practice pentru adultul cu îngrijorări neuro-trofice subclinice
Cele care urmează nu sunt prescripții medicale. Sunt sinteza dozelor și a protocoalelor de coama leului folosite în studiile care au generat evidența pozitivă pentru populația 40–65 ani cu plângeri subclinice pe memoria de lucru, viteza de procesare cognitivă și/sau recovery lent neuromuscular post-trauma minor, fără patologie neurologică majoră declarată.
Doză. Studiile cu efect pozitiv pe cogniție au folosit 1–3 g/zi pulbere de coama leului sau echivalent în extracte concentrate. Mori 2009 a folosit 3 g/zi pulbere ne-standardizată; Docherty 2023 a folosit 1.8 g/zi extract concentrat[3][5]. Pentru formulările concentrate 20:1 cu standardizare cuantificată pe hericenone, doza echivalentă în mg poate fi semnificativ mai mică prin densificarea bioactivilor — recomandarea practică este să compari mg-cu-mg conținutul de hericenone standardizat (nu masa extractului) între produse.
Durată minimă. Sub 8 săptămâni efectul cognitiv este inconstant. RCT-urile cu rezultate pozitive au avut durate de 8–16 săptămâni[3][4][5]. Recomandare conservatoare: 12 săptămâni înainte de evaluarea subiectivă a efectului, apoi decizie informată privind continuarea. Pentru susținerea recovery-ului neuromuscular post-leziune, modelele animale sugerează că administrarea precoce (în primele săptămâni post-injury) este mai eficientă decât administrarea tardivă, dar acest pattern nu a fost încă replicat uman.
Monitorizare. Nu există un biomarker plasmatic standard pentru efectul coama leului. Evaluarea se face subiectiv (auto-percepție memorie, focus, energie cognitivă) și, dacă există plângeri specifice, prin testare cognitivă formală făcută de un specialist (psiholog cognitiv, neurolog). Pentru profilul de siguranță hepatic, transaminaze (ALT, AST) la baseline și la 12 săptămâni dacă există co-medicație cronică sau patologie hepatică preexistentă.
Cu cine să discuți înainte. Cu medicul de familie sau cu neurologul, în special dacă: ai medicație cronică (interacțiunile farmacocinetice cu coama leului nu sunt complet cartografiate), ești sub anticoagulant (efectul antiplachetar in vitro al unor compuși fungici nu este clarificat clinic), ai boală autoimună activă (stimularea imună prin beta-glucan), ai diagnostic neurologic stabilit (Alzheimer, Parkinson, scleroză multiplă, neuropatie diabetică declarată) — în aceste cazuri coama leului nu înlocuiește terapia indicată, iar coordonarea cu medicul curant este obligatorie.
Stil de viață concomitent. Cea mai puternică evidență pentru menținerea funcției cognitive subclinice rămâne combinația somn 7–8 h pe noapte, activitate fizică aerobă moderată (≥150 min/săpt), dietă bogată în acizi grași omega-3 și polifenoli, învățare continuă (activitate cognitivă nouă). Coama leului nu înlocuiește aceste intervenții — le poate compensa parțial la nivel biochimic, dar nu structural. Pentru regenerare neuromusculară, fizioterapie țintită + protein intake adecvat + somn sunt prioritare.
Întrebări care decurg din analiza dovezilor
Este coama leului un tratament pentru Alzheimer sau pentru demență stabilită?
Nu. RCT-ul Mori 2009 a fost pe pacienți cu Mild Cognitive Impairment (MCI) — un stadiu pre-demență cu deficit cognitiv ușor obiectivabil, dar fără criteriile diagnostice pentru Alzheimer sau demență vasculară. Niciun trial uman publicat indexat nu a testat coama leului ca intervenție în demență stabilită cu rezultate pozitive replicate. Pentru pacienții cu diagnostic neurologic de demență, terapia este coordonată de neurolog/psihiatru — coama leului nu este o alternativă la inhibitorii de acetilcolinesterază sau la memantină[3][10].
Cât durează până se observă diferența?
În RCT-urile umane, semnale pozitive au apărut la 8–12 săptămâni de administrare consecventă. Docherty 2023 a observat efect acut subiectiv pe stres după o singură doză, dar efectele cognitive obiectivabile au necesitat 28 de zile[5]. Pentru regenerarea axonală, modelele animale arată că efectul se acumulează pe parcursul a 4–8 săptămâni post-injury. Recomandarea practică: minimum 8 săptămâni înainte de a evalua dacă există vreun efect personal observabil.
De ce diferă atât doza producători (sub 1 g/zi) de doza din studii (1–3 g/zi)?
Studiile clasice (Mori 2009) au folosit pulbere ne-standardizată — o doză mare în masă este necesară pentru a livra o cantitate suficientă de bioactivi cuantificați. Formulările moderne 20:1 cu standardizare HPLC pe hericenone livrează aceeași cantitate de compuși activi într-o masă semnificativ mai mică. Nu compara mg-cu-mg între pulbere și extract concentrat — compară conținutul de hericenone (sau de erinacine, dacă este miceliu) standardizat pe etichetă[10]. Datele directe de bioechivalență între formulări lipsesc din literatura publicată.
Care este profilul persoanei care răspunde cel mai bine?
Conform sintezei RCT-urilor și revizii sistemice Menon 2025, profilul „responder” pe latura cognitivă este: 40–80 ani, cu plângeri subiective de declin cognitiv ușor sau cu MCI confirmat, fără demență declarată, fără patologie hepatică majoră. Pentru regenerare neuromusculară, datele umane sunt insuficiente pentru a defini un profil — modelele animale sugerează că administrarea precoce post-leziune (primele 1–4 săptămâni) și absența diabetului zaharat decompensat (care afectează regenerarea axonală indiferent de intervenție) sunt factori favorabili[4][10].
Există interacțiuni medicamentoase importante?
Datele sunt limitate. In vitro, unele compuși fungici au activitate antiplachetară ușoară — relevanța clinică la doze nutraceutice este probabil mică, dar prudența este obligatorie la pacienții pe anticoagulant (warfarină, acenocumarol, NOAC). La pacienții pe imunosupresoare (după transplant, în boli autoimune), stimularea imună prin beta-glucan poate teoretic interfera — coordonare obligatorie cu medicul curant. Ghidul National Cancer Institute — Complementary and Alternative Medicine oferă perspectiva oncologică pe interacțiunile medicamentoase ale suplimentelor de origine fungică în contextul terapiilor sistemice.
Profilul tehnic al unei formulări standardizate triplu
Pentru cititorul care vrea să evalueze critic un supliment de coama leului din piață, există trei parametri tehnici care deosebesc o formulare bine documentată de una opacă: (1) tipul extractului (corp fructifer vs miceliu vs combinație), (2) raportul de extracție (1:1 pulbere → 20:1 sau mai mult), (3) standardizarea cuantificată pe bioactivi specifici (hericenone B–H pentru fruiting body; erinacine A–I pentru miceliu) prin HPLC, NU doar pe polizaharide totale. Majoritatea suplimentelor românești și europene standardizează doar pe polizaharide totale — un marker generic care nu distinge bioactivii relevanți pentru efectele neurotrofice.
Ca exemplu de formulare cu standardizare triplă (polizaharide ≥50% + beta-glucan ≥30% + hericenone ≥2.5%) pe piața românească, produsul Coama Leului BioCORE® PureOrganics conține 450 mg extract corp fructifer Hericium erinaceus 20:1 per porție, cu cuantificarea celor trei markeri menționați. Hericenonele B–H reprezintă ~11 mg per porție — cantitatea care permite compararea mg-cu-mg cu bioactivii din studii. Tehnologia BioCORE® (Science of Life PHARMA) este un sistem de transport liposolubil care urmărește să îmbunătățească absorbția hericenonelor (lipofile prin natura lor chimică); literatura publică pe sisteme similare (fitozomi, complexe lipidice) sugerează biodisponibilitate mai mare față de extract liber, dar studii pK proprii pentru BioCORE® coama leului nu sunt publicate independent.
Testarea independentă pe lot (HPLC pentru standardizare, microbiologie pentru E. coli/Salmonella/mucegaiuri, metale grele Pb/Cd/As/Hg sub limitele UE pentru suplimente alimentare, reziduuri pesticide multireziduuale) este standardul minim de calitate pentru un supliment. Aceste teste verifică ceea ce eticheta promite și ceea ce literatura asociază cu efectele observate. Pentru alte ghiduri de ingrediente analizate cu același pattern, vezi colecția de ghiduri PureOrganics.
Concluzie
Coama leului nu este nici „nootropic universal”, nici „remediu pentru neuropatii”. Este o ciupercă medicinală cu bioactivi standardizabili (hericenone B–H, erinacine A–I) care stimulează o cale neurotrofică (NGF–TrkA–ERK1/2) implicată simultan în susținerea memoriei centrale și în regenerarea axonală periferică. Pentru adultul de 40–65 ani cu plângeri subclinice pe memoria de lucru, viteza de procesare cognitivă și/sau recovery lent neuromuscular minor, coama leului la 1–3 g/zi pulbere (sau echivalent în extract standardizat) timp de minimum 8–12 săptămâni are bazinul de evidență cel mai solid pe latura cognitivă, cu suport pre-clinic robust pe latura periferică. Pentru oricine altcineva — la vârste extreme, cu boală neurologică majoră, cu așteptarea unui efect rapid sau ca alternativă la terapie specifică —, alegerea informată cere conversație cu medicul curant și acceptarea că dovezile umane sunt mai puține decât pare la prima căutare online.
Revizuit medical de: Simon Andrei (founder Science of Life PHARMA, ORCID 0009-0005-7945-106X). Ultima revizie: 12 mai 2026. Următoarea revizie planificată: 12 noiembrie 2026.
Conținutul ghidurilor este revizuit periodic pentru actualizare cu literatura recentă. Standardele de calitate și revizie · Profilul recensorului medical.
Surse
- Martínez-Mármol R, et al. (2023). Hericerin derivatives activates a pan-neurotrophic pathway in central hippocampal neurons converging to ERK1/2 signaling enhancing spatial memory. Journal of Neurochemistry, 165(6):791–808. PMID: 36660878. doi:10.1111/jnc.15767
- Szućko-Kociuba I, et al. (2023). Neurotrophic and Neuroprotective Effects of Hericium erinaceus. International Journal of Molecular Sciences, 24(21):15960. PMID: 37958943. doi:10.3390/ijms242115960
- Mori K, et al. (2009). Improving effects of the mushroom Yamabushitake (Hericium erinaceus) on mild cognitive impairment: a double-blind placebo-controlled clinical trial. Phytotherapy Research, 23(3):367–372. PMID: 18844328. doi:10.1002/ptr.2634
- Saitsu Y, et al. (2019). Improvement of cognitive functions by oral intake of Hericium erinaceus. Biomedical Research (Tokyo), 40(4):125–131. PMID: 31413233. doi:10.2220/biomedres.40.125
- Docherty S, et al. (2023). The Acute and Chronic Effects of Lion’s Mane Mushroom Supplementation on Cognitive Function, Stress and Mood in Young Adults: A Double-Blind, Parallel Groups, Pilot Study. Nutrients, 15(22):4842. PMID: 38004235. doi:10.3390/nu15224842
- Taib NAB, Eshak ZB. (2026). Application of Medicinal Mushrooms for the Treatment of Peripheral Nerve Injury: A Systematic Review. (Indexed PubMed). PMID: 41562932
- Yow YY, Goh TK. (2021). Therapeutic Potential of Complementary and Alternative Medicines in Peripheral Nerve Regeneration: A Systematic Review. Evidence-Based Complementary and Alternative Medicine. PMID: 34571842
- Wong KH, et al. (2016). Hericium erinaceus (Bull.: Fr.) Pers., a medicinal mushroom, activates peripheral nerve regeneration. Chinese Journal of Integrative Medicine. PMID: 25159861
- Wong KH, et al. (2011). Peripheral Nerve Regeneration Following Crush Injury to Rat Peroneal Nerve by Aqueous Extract of Medicinal Mushroom Hericium erinaceus. Evidence-Based Complementary and Alternative Medicine, 580752. PMID: 21941586
- Menon A, Jalal A. (2025). Benefits, side effects, and uses of Hericium erinaceus as a supplement: a systematic review. (Indexed PubMed). PMID: 40959699
Acest ghid are scop informativ. Informația din literatura citată nu înlocuiește consultul medical individualizat. Pentru decizii terapeutice — în special în prezența unei afecțiuni neurologice declarate, a medicației cronice sau a sarcinii — consultați medicul curant sau neurologul.

